
釋義???預混與共處理藥用輔料?Pre-mixed or Co-processed excipient
預混與共處理藥用輔料系將兩種或兩種以上藥用輔料按特定的配比和工藝制成具有一定功能的混合物���,作為一個輔料整體在制劑中使用���。既保持每種單一輔料的化學性質�����,又不改變其安全性�����。根據處理方式的不同����,分為預混輔料與共處理輔料��。
預混輔料(Pre-mixed excipient)系指兩種或兩種以上藥用輔料通過簡單物理混合制成的�、具有一定功能的且表觀均一的混合輔料�����。預混輔料中各組分仍保持獨立的化學實體�。
共處理輔料(Co-processed excipient)系由兩種或兩種以上藥用輔料經特定的物理加工工藝(如噴霧干燥����、制粒等)處理制得�����,以達到特定功能的混合輔料����。共處理輔料在加工過程中不應形成新的化學共價鍵�。與預混輔料的區別在于���,共處理輔料無法通過簡單的物理混合方式制備�����。
隨著眾多新型藥物制劑的誕生��,其多變的理化性質以及對穩定性的要求���;新的設備和生產工藝的出現����;新的法規對穩定性����、安全性的要求���;對輔料的功能提出了更多��、更高的標準�����,使得現有的一些單一輔料已經不能滿足發展要求���。

預混
預混輔料是由多種單一輔料經特定的加工工藝混合而成����,各生產企業的配方組成及加工工藝各不相同�,相應的質量標準也是不同的��。但目前同類預混輔料的通用名稱大多相同�����。如市場上廣泛應用的薄膜包衣預混劑�,國內外有多家企業生產����,各自擁有不同的配方����,由于名稱相同�����,許多使用單位將其認定為相同品種�����,用相同的質量標準去衡量�。但預混輔料并不是幾種單一輔料的簡單任意混合����,這個過程仍然是復雜的��,因為每種輔料都可能和其他輔料發生相互作用��。它是經過專業的技術人員不斷地探索和研究�,如同新藥開發一樣����,需要大量的處方篩選�,尋找各種性能適合的單一輔料��,不斷地調整輔料之間的比例�����,每一步還需要通過嚴格的性能測試����,穩定性考察�����,同時還要考慮其與各種活性藥物的兼容性����,最終獲得一個滿足技術要求的完善的配方�。
對于藥品研發人員來說��,直接使用預混輔料�,不僅可以賦予制劑產品許多新的功能����,還可以省略掉相當一部分的處方篩選工作�����。我們只需要了解某一種預混輔料的特點��,并適當的加以運用�,就可達到原來使用多種輔料反復調配才能達到的效果�����,大大地縮短了研發周期���。
對于生產廠家來說��,原來多種輔料反復地采購�,質量檢驗�����,儲存等大量的工作��,都被單一的預混輔料代替��,大大提高了生產效率��,降低了生產成本���。
如今傳統的片劑采用蔗糖包衣的方法基本退出市場�。薄膜包衣預混劑由成膜材料�����、增塑劑��、填充劑和色素等構成����,外觀上是顏色一致的均勻粉末��,進行片劑包衣時比蔗糖包衣簡單方便����,并降低了片劑的質量和體積�。預混包衣輔料中加入其他合適的輔料��,可以增強防潮���、改善外觀�����、掩蓋藥物不良氣味��、調整口感等各種性能���,并可以滿足藥物腸溶�、胃溶或者控釋要求���。

由于高速壓片機的出現和直接壓片方法的使用�����,對輔料功能的要求也與日俱增����。協同加工在開發具有多功能活性的穩定藥用輔料方面起著重要作用�����。人們對一種或兩種天然或合成聚合物的組合進行了廣泛的探索�,以開發新型穩定的共處理藥用輔料��。預混與共處理藥用輔料是在傳統輔料基礎上開發制得的新型輔料�,具開發周期短��、生產簡便����、具特定功能性且質量穩定等特點���,有著較好的應用前景�。
1986年FMC公司申請了第一個微晶纖維素與碳酸鈣共處理輔料�,共處理輔料(Co-processed excipient)的概念被首次提出���。此后多家國際著名藥用輔料生產商開始研究和開發預混與共處理藥用輔料�。目前�,多種共處理輔料已被成功開發并應用于多種藥物制劑的生產中�,如法國Roquette公司的甘露醇淀粉復合物(Pearlitol Flash)���,德國Meggle公司的纖維素乳糖80(Cellactose 80)�����,德國BASF公司的乳糖�、聚維酮和交聚維酮直壓共處理輔料(Ludipress)�����、德國JRS公司的硅化微晶纖維素(Prosolv)系列和美國FMC公司的微晶纖維素-羧甲纖維素鈉(Avicel RC/CL)等��。隨著國內藥物制劑研發水平的提升�����,對制劑工藝及新型輔料的需求不斷提高�����,近年來國內輔料企業也著力于共處理藥用輔料的研制��。
1.?共處理輔料的制備方法
一���、噴霧干燥
與單個輔料或其物理混合物相比��,噴霧干燥制備的復合輔料流動性�、吸濕性���、可壓性等性能有明顯改善�����,其顆粒性質可控��,易于規?����;a����,是制備高功能輔料應用最為廣泛且較為成熟的一項技術���。藥物溶液或混懸液均勻噴霧于熱的干燥室內�����,隨著液滴表面積和溫度的升高�����,液滴中的水分迅速蒸發�����,形成可用于直接壓片的半球形中空粒子�����。操作過程中應精確控制各種噴霧干燥工藝參數�����,如入口空氣溫度��、霧化空氣壓力���、進料速率和固體進料的體積等���,這對于顆粒所需性能設計至關重要�。將輔料溶液或混懸液噴霧于干燥室內�,隨著液滴表面積和溫度升高�,液滴中水分迅速蒸發�����,形成球狀顆粒�。入口空氣溫度���、霧化空氣壓力�����、進料速率和體積等工藝參數相對重要�����,噴霧干燥制備的混合輔料流動性�、吸濕性���、可壓性等性能有明顯改善�����,是應用最為廣泛且成熟的一項技術����。? ??
二�����、流化床制粒? ?
流化床制粒主要通過氣流使輔料保持流化狀態����,再將輔料溶液或混懸液由上部向流化室內噴入�����,使粉末聚結成顆粒���。通過該方法形成的顆粒形狀與噴霧干燥基本一致���,其主要區別在于前者顆粒流動性較差��,且粒度分布較不規則����。?
三�、干法制粒/濕法制粒? ? ?
干法制粒是將輔料混合后��,靠壓縮力制成胚片����,再經整?��;蜻^篩至合適的粒徑�。濕法制粒是將輔料混合后制成軟材�,再經整?��;蜻^篩至合適的粒徑��。與噴霧干燥或流化床法相比�,該法制得的顆粒流動性較差��,孔隙率較小����,但可壓性往往更佳���。
四�、共沉淀技術
共沉淀通常是將塑性和彈性輔料溶解于揮發性溶劑中����,在65~700℃下用磁力攪拌器攪拌至溶劑完全蒸發����,最后將所得濕的凝聚物過篩�、干燥�。該方法可明顯改善輔料的可壓性和流動性��。應用共沉淀技術開發的直接壓片輔料甲殼素和二氧化硅復合物���,電鏡掃描顯示����,殼多糖微粒涂覆于二氧化硅內部使兩者緊密的整合在一起����。該復合輔料可壓性和稀釋性良好����,其高吸濕性和高滲透性使其崩解性也極大的改善�。
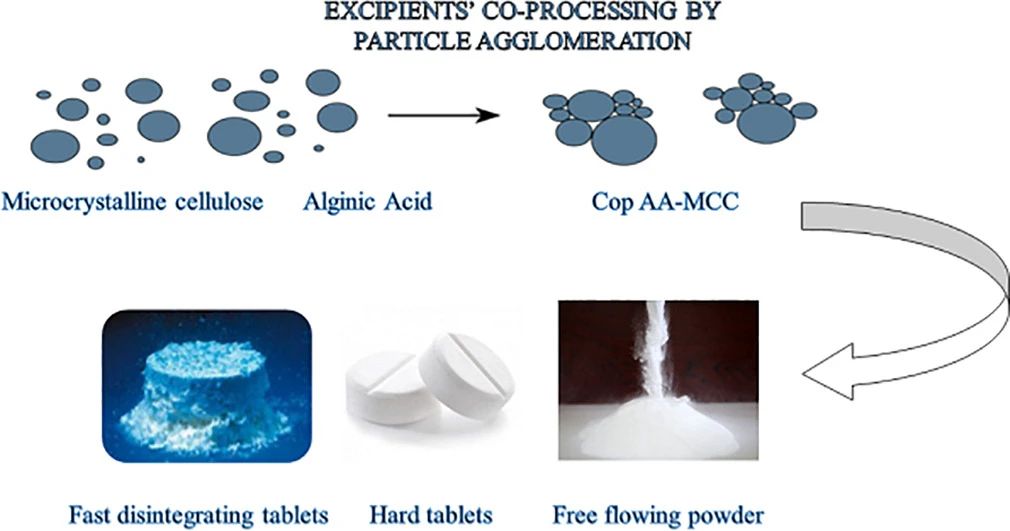
盡管共處理輔料的優勢已被證實�����,制藥業的部分人士仍然不愿意接受共處理�,部分原因是他們在不知情的情況下認為使用共處理輔料會增加監管風險����,而且監管當局會要求進行額外的安全測試����。共處理賦形劑已經存在多年了�����。1985年��,Ludipress? (BASF)是最早為口服固體制劑設計的賦形劑之一����。硅化微晶纖維素是在1996年推出的����。在過去的25年里���,共同加工的材料和等級的數量已經大大增加����。
在某些情況下��,使用共同加工的輔料提高了成品的堅固性�����,減少了產品失敗的發生率���。例如��,在一種可壓縮性差的散裝活性物質(API)的片劑配方中����,每一批都必須檢查是否有損壞的片劑����,而損壞的�、被拒絕的片劑數量約為15-20%��。使用由配方中已有的輔料組成的輔助加工輔料�����,通過提高配方的密實度���,消除了受損片劑��。然后�,制造商能夠取消人工檢查����,從而降低成本�。更重要的是���,該配方和工藝更加穩定����。營養品領域也有這樣的例子�����,使用共同加工的輔料使高劑量�、難壓實的營養補充劑的片劑配方更加堅固����,使用的輔料量更少���,從而使患者更容易獲得小片劑�����。
隨著人們對連續生產藥品成品的興趣增加--特別是口服固體制劑--已經開始限制成分的數量�,因為在任何時候可以進入連續生產設備列車的輔料數量有限����。在我看來��,這反過來又導致了過度簡化的配方的增加�。
如果在開發連續生產的產品和工藝時沒有充分考慮到配方和工藝的穩健性�����,那么連續生產的好處就可能無法實現���,因為滿足規格的故障增加���。在一個特定的制造列車中�,對材料進料斗數量的限制可能是有問題的�����;它限制了在任何一個時間內可以進入設備列車的材料數量�����。
一個解決方案���?包括一個預混合的步驟����,這將允許額外的進料系統���。然而���,這意味著至少要集成一個額外的單元工藝和相關的喂料器�。這將增加資本和開發成本����。
對于口服固體制劑的連續生產線�,一個替代方案是使用共同加工的賦形劑���,如填充劑和超級分解劑的共同加工組合��,或填充劑�����、超級分解劑和壓實增強劑的組合���。這將需要較少的藥物產品生產過程中的材料進料器��,從而使生產設備列車更簡單�����。目前有一些等級的共處理輔料���,包括這樣的材料組合����,可供制藥和營養品使用��。
有些人認為�����,根據2005年的新輔料非臨床測試指南����,FDA將要求對共處理輔料進行額外的安全測試�,因為有可能形成新的共價化合物�����。這是不正確的! 使用一系列的分析技術可以證明不存在新的共價鍵材料����。Tobyn等人(1998年)對硅化的微晶纖維素證明了這一點���。這種一般方法可以根據需要進行調整���,并用于其他共處理輔料�����,以證明共處理后沒有新的共價鍵實體�����。反過來�����,這將允許與共處理賦形劑中的成分賦形劑的安全數據和/或安全使用歷史相銜接���,這將節省大量費用和時間�。
在歐洲出現了另一個監管問題��。一些監管者認為�,共同加工規避了現行的良好生產規范(cGMPs)����?���?梢哉f���,這種想法與歐洲的法規相悖�����。歐洲假藥指令(FMD)將輔料納入歐洲藥品法規的管轄范圍�����,并包括一項要求�,即藥品制造商對適用于其輔料生產的良好生產規范的適當性進行正式的風險評估���。關于正式風險評估程序的指南已于2015年發布����。因此�,輔料使用者必須評估輔料生產商對GMP的應用����,以確定所應用的GMP標準是否適合于輔料的預期用途���。這些監管機構的態度似乎暗示輔料的GMP不如成品的GMP��。事實并非如此�����。全球公認的GMP標準適用于輔料(例如��,見ANSI 363�,WHO附件5和EXCiPACT)���。
舉個例子來解釋這個矛盾����,考慮一下通過直接壓縮制成的片劑��,包括藥物���、填充劑(如微晶纖維素)和潤滑劑(如硬脂酸鎂)�����。(這與上面關于過度簡化的例子相似�����。)只要銷售申請可以接受�,沒有理由不批準這種制劑上市��。然后考慮一種片劑配方����,也是通過直接壓縮制成的�,包括一種藥物��、一種共同加工的填充物(如硅化微晶纖維素)和一種潤滑劑(如硬脂酸鎂)���。不知何故��,根據那些某些監管機構的想法����,這種配方不應該被批準��,因為它含有一種共同加工的賦形劑�,那些監管機構認為這種賦形劑的生產標準低于cGMP標準���。制造硅化微晶纖維素的輔料制造商也制造微晶纖維素���,而且很可能按照相同的GMP標準生產這兩種輔料�����。那么����,為什么微晶纖維素在這種應用中可以被接受����,而硅化微晶纖維素卻不能�����?
總之�,共同加工的輔料在提高醫藥產品和工藝的穩健性方面有著巨大的潛力���。此外����,它們還有可能促進醫藥成品更穩健和更簡單的連續生產��。然而��,要實現這一潛力�,制藥商和監管當局都必須接受共處理輔料不會帶來不必要的監管風險�����,并且是輔料武器庫中的合法補充����。共處理賦形劑的開發者和制造商將需要進行必要的研究���,以證明共處理賦形劑在特定應用范圍內是安全����、有效和穩定的�����。
應用案例一:
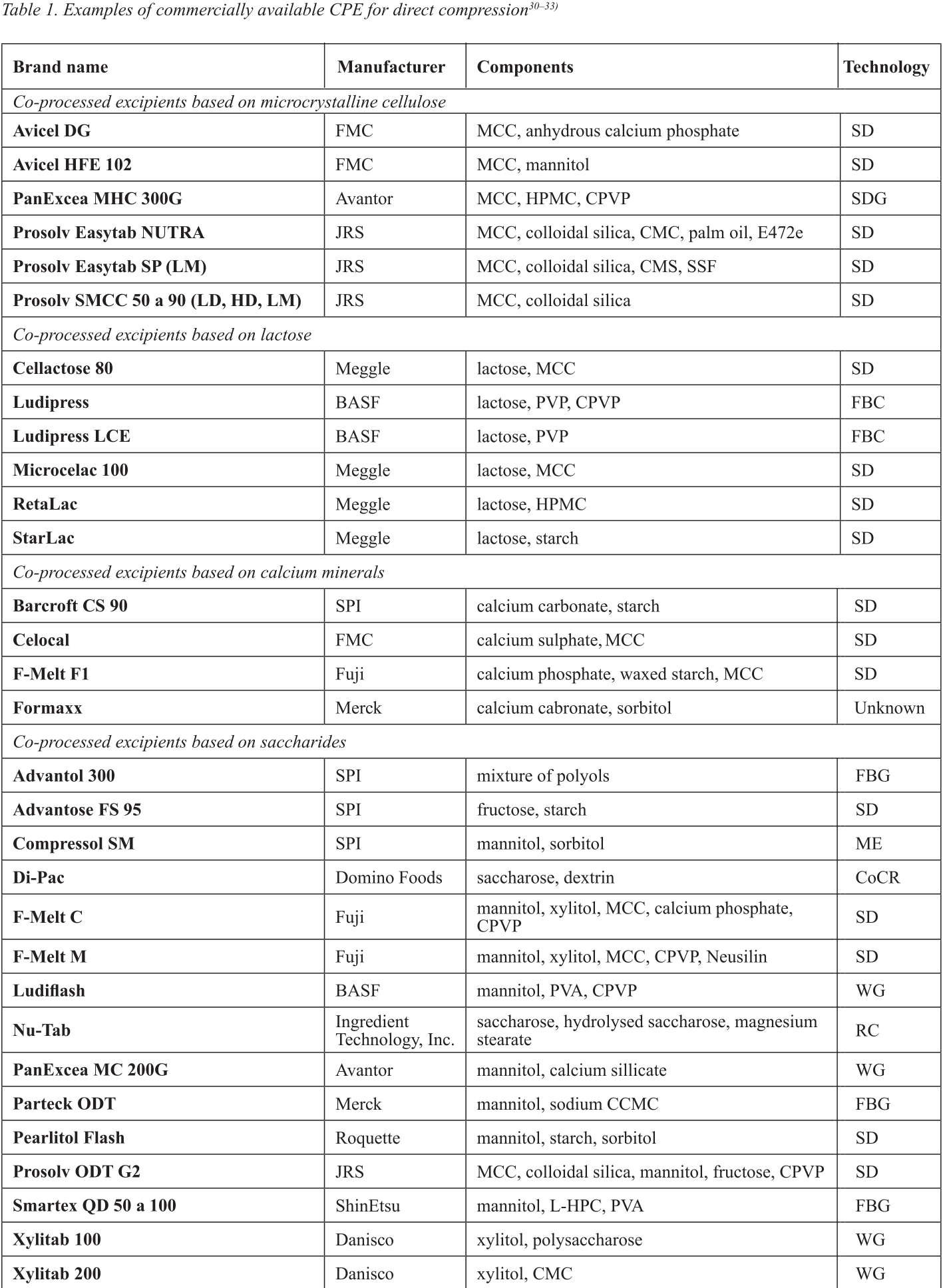
用于直接壓片的共處理輔料(CPE)

片劑是最經常使用的劑型��。它們的優勢在于可獲得性�����、易于服用��、穩定性好和價格低廉��。生產片劑最簡單的技術是直接壓片����,盡管使用這種方法需要克服許多障礙�����,主要涉及內容的均勻性和質量的變化�、崩解����、溶出和片劑的徑向硬度����。
含有填充劑��、粘合劑����、崩解劑�、潤滑劑和其他輔料的共同加工混合物的 '共同加工輔料 '如今被越來越廣泛地使用����。這些混合物是通過各種技術制造的����,主要是通過噴霧干燥��、流化床造粒�����、濕法造粒�、熔融造粒���、干法造粒和共結晶等�。
用于直接壓片的共處理藥用輔料
應用案例二:
共處理輔料類型對含有卡托普利����、曲馬多和多潘立酮的口崩片(ODTs)性能的影響
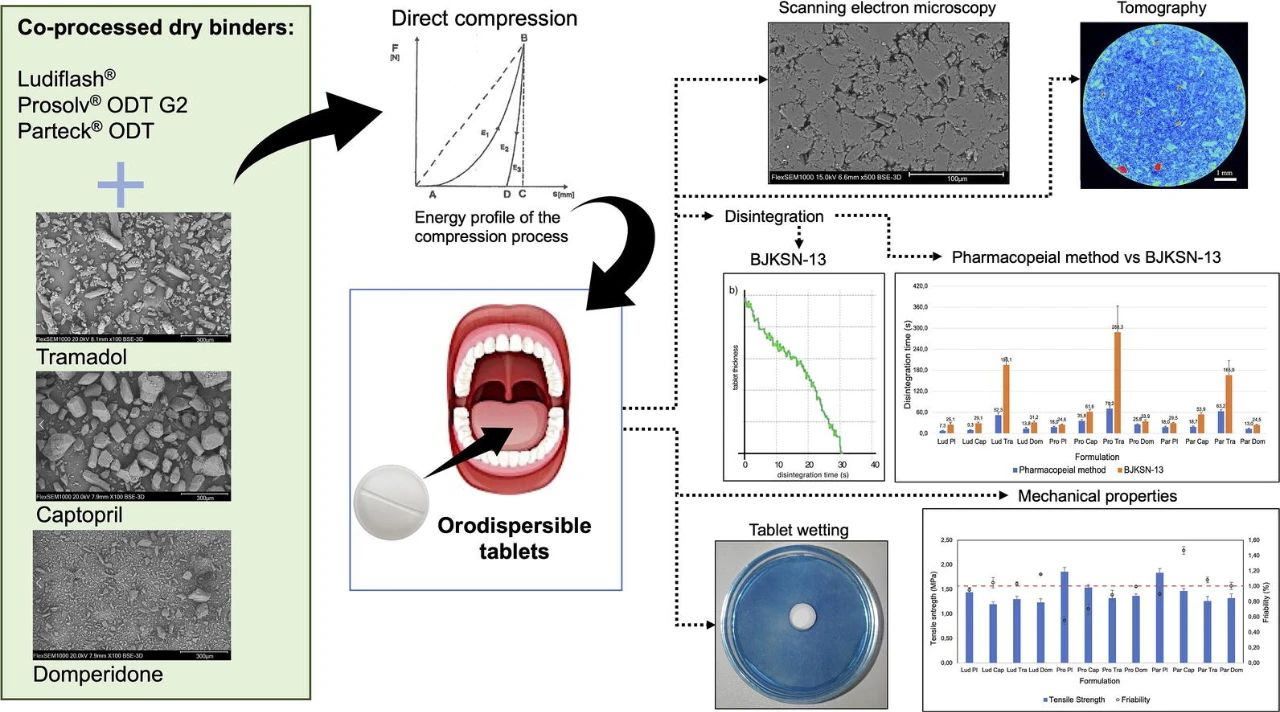
口服分散片(ODTs)的一個重要特點是給藥方便��,在某些情況下���,起效更快����,穩定性保持��,劑量精確���。這項工作的重點是通過直接壓片法制備含有甘露醇基輔料Prosolv? ODT G2���、Ludiflash?和Parteck? ODT與曲馬多��、卡托普利和多潘立酮組合的ODT��。
亮點
?? 利用共處理輔料成功制備了口服分散片�。
?? Prosolv? ODT G2為所研究的API提供了高質量的口服分散片���。
?? 通過Ph.Eur.方法和BJKSN-13儀器得到不同的崩解時間���。
Prosolv? ODT G2由于含有微晶纖維素而顯示出高的塑性變形能量�����。Parteck? ODT由于含有顆粒狀的甘露醇而提供了緊湊的片劑�����。所有藥物都降低了拉伸強度�����,增加了易碎性�,延長了崩解時間��,并降低了片劑的孔隙率��。含有Prosolv? ODT G2與卡托普利��、多潘立酮和曲馬多�����;以及Parteck? ODT與多潘立酮的片劑符合ODTs的生產要求��,即易碎性≤1%�����,崩解時間≤180秒��,潤濕時間快�,吸水率高���,抗張強度足夠���。崩解時間用藥典方法和BJKSN-13儀器進行了測試���。結果表明�����,這些方法之間存在著明顯的差異�,用BJKSN-13儀器測試時�,崩解時間更長��。
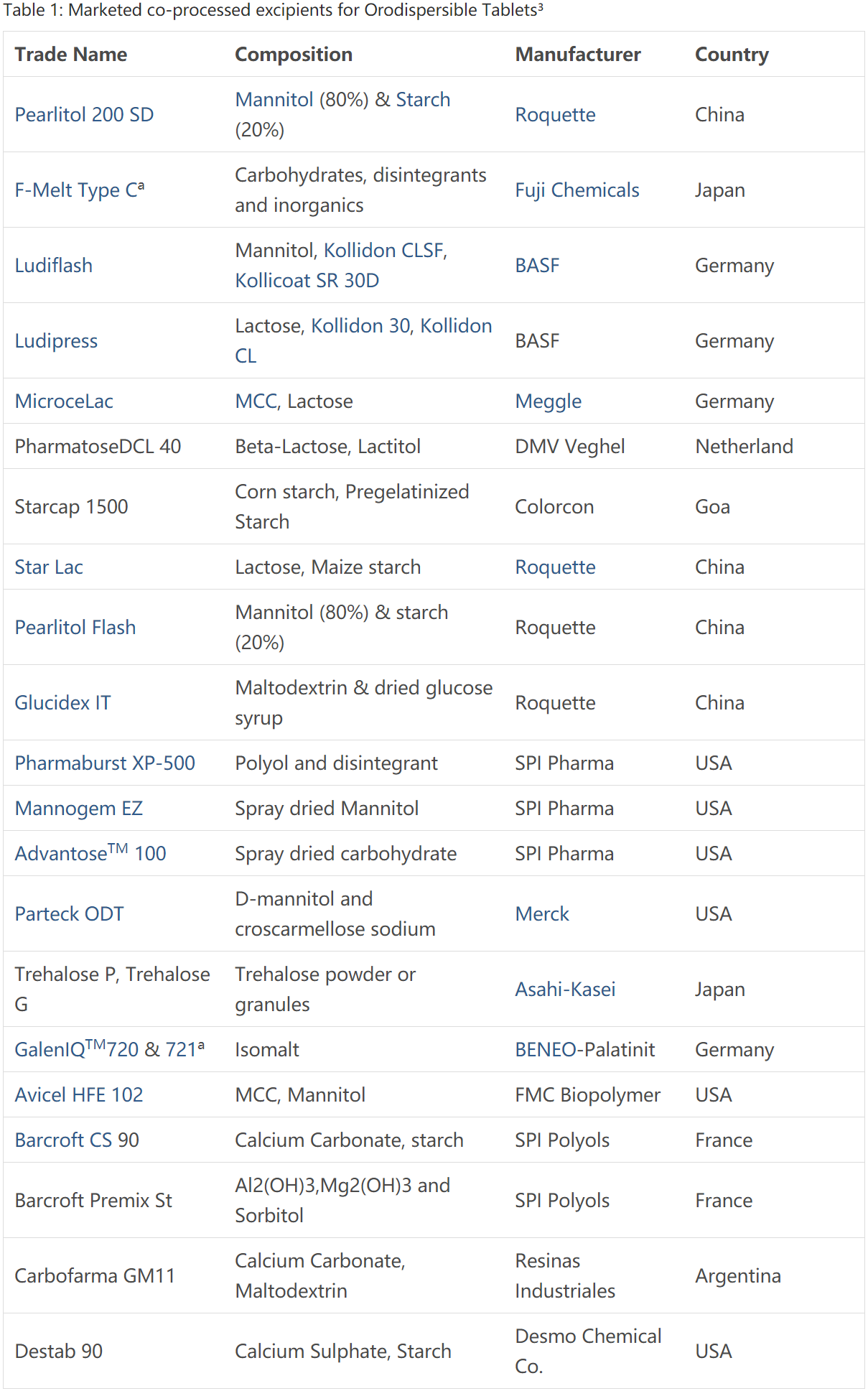
口崩片中應用的已上市共處理藥用輔料
2015年12月31日�����,歐洲藥典新章節草案“預混輔料”在27.4中公布����,在擬定的章節中�,預混輔料定義為“兩種或更多種輔料通過物理預混獲得的混合物���,其中不含有分子鍵”���。用于預混的單個輔料必須符合歐洲藥典中相應的各論要求�,以及藥用物質的通論要求����。另外����,預混輔料還要符合藥用物質通論的要求��。預混輔料可以通過只會發生物理反應的工藝過程制得�����,例如�����,共同干燥��,噴霧干燥�,制粒���,擠出和高剪切分散��。這些工藝可以是間歇生產也可以是連續工藝����。所擬的各論包括部分為屬性����、鑒別���、測試�����、含量�����、標簽和功能性相關特性����。在“測試”部分提議“為最終預混物料整體質量定義質量標準”��,“如果預混輔料包括了單成分各論中未受控的雜質����,則必須指明并進行適當控制”�。
2019年7月26日�,國家藥典委員會擬制定《預混與共處理藥用輔料質量控制指導原則》�����,并收載于《中國藥典》四部��。該指導原則的發布彌補了我國對預混與共處理藥用輔料在法規層面和技術層面的空白���,也充分體現出市場對新型藥用輔料研發應用的迫切需求���。
指導原則:
預混與共處理藥用輔料(以下簡稱產品)及其各組分應滿足藥用要求���;產品生產應建立相應的質量管理體系�,并滿足制劑的要求����;產品配方設計和工藝參數選擇應滿足產品的特點和預期功能�。
預混輔料在生產過程中應對剪切速度等關鍵工藝參數進行充分驗證�����,并按驗證后的工藝參數生產�����,以確保產品的均一性�����,尤其應關注配方中較低組分的均一性��。共處理輔料應充分評估配方的合理性和工藝條件的科學性��,以達到預期功能�,且在生產過程中不形成新的化學共價鍵����;應基于單一組分的安全性�,結合工藝過程��,評估產品的安全性��。
應根據配方組成���、生產工藝�、預期功能以及配方組分中各單一組分的特性等����,建立反映產品安全性����、功能性與質量均一性的檢測項目��,其質量研究與控制包括但不限于以下方面:
一���、性狀 從色澤���、外觀和溶解性等對產品的性狀進行描述���。
二�����、鑒別 采用紅外光譜�����、拉曼光譜����、液相色譜等適宜的方法�����,對配方中的關鍵組分進行鑒別��。
三�����、檢查 應根據產品的配方和工藝�,建立檢查項目��,如干燥失重���、水分�����、殘留溶劑�����、熾灼殘渣(或灰分)�����、重金屬(或元素雜質)與有關物質等�����。對于共處理輔料�,若工藝處理后出現了配方中單一組分雜質譜以外的新雜質�,應對其進行結構確證�,并對其安全性進行充分評估���,同時應關注生產過程中可能發生的晶型變化等問題��。
四����、功能性指標?采用適宜的方法����,有針對性地建立適合預期功能的關鍵功能性檢查項目���,如色差�����、腸溶崩解性能�����、黏度��、粒度與粒度分布���、流動性等��。
五����、含量 及功能有效性指標 對于共處理輔料中各組分�����,以及預混輔料中含量變化可顯著影響產品功能性的組分�����,應盡可能建立有效的分析方法測定其含量或其他反映其功能有效性的指標��。
六����、微生物限度 必要時���,應建立適宜的方法檢查產品的微生物限度���。限度應符合藥用輔料的要求����,并滿足所應用的制劑要求�。
七�、穩定性研究 模擬市售包裝����,選擇適宜的考察條件進行穩定性研究��,考察內容除化學穩定性與物理穩定性外�,應重點關注產品的功能性指標���。共處理輔料還需關注晶型(如有)與雜質(包括單一成分控制的雜質及其之外的新雜質)等的變化情況��。根據產品特點與穩定性考察結果���,選擇適宜的包裝材料和貯藏條件�,以確保產品質量穩定��。
中國藥用輔料通用名稱命名原則中����,預混輔料與共處理輔料是對兩種或兩種以上輔料通過不同處理方式獲得的輔料混合物�,在命名中應予以體現����。
命名原則:
(1)預混輔料一般是多種輔料的簡單物理混合物���,在中文通用名后加“預混物”����,英文名前加“pre-mixed”��。通常按用途命名�����,如薄膜包衣預混物(胃溶型)�、薄膜包衣預混物(含乳糖)�����、薄膜包衣預混物(腸溶型)等�����。若只有兩個組分�����,采用兩個組分的全稱疊加���,再加預混物���,組分疊加順序根據組分質量比由大到小排序��。
(2)共處理輔料不是簡單的物理混合物�,一般由兩個或兩個以上輔料共加工處理形成�,輔料的物理特性發生了改變但化學特性無明顯變化����。
中文通用名一般為組分疊加后加“共處理物”��,組分疊加次序根據共處理輔料中組分的質量比由大到小排序�;當組分比例一致時�����,根據其英文名首字母次序排序�;當組分超過兩個時����,為避免中文通用名過長�,比例在 2%以下的組分可不在名稱中體現�����,但應在來源與定義中描述���。
英文名通常為“Co-processed”加組分疊加��,應將全部組分列出��,每個組分之間用逗號間隔���,最后兩個組分用 and 相隔�����。
①? 兩個組分的共處理輔料��,中文通用名以兩個組分的全稱疊加�����。如微晶纖維素膠態二氧化硅共處理物(曾用名:硅化微晶纖維素)�,Co-processed Microcrystalline Cellulose and Colloidal Silicon Dioxide ( 曾 用 名 :Silicified Microcrystalline Cellulose)�����;乳糖聚維酮共處理物�,Co-processed Lactose and Povidone�。
②? 三個或三個組分以上的共處理輔料����,中文通用名第一個組分采用全稱���,之后的組分可采用縮詞法����,選詞見所附縮詞表及選詞原則 ����。如 乳 糖 微 晶 淀 粉 共 處 理 物 �, Co-processed Lactose,
Microcrystalline Cellulose and Starch(備注:一水乳糖 70%���、微晶纖維素 20%�、玉米淀粉 10%)���;乳糖交聚聚維酮共處理物���,Co-processed Lactose,Crospovidone and Povidone(備注:一水乳糖93%�、交聯聚維酮 3.5%�、聚維酮 3.5%)�。
選詞原則:共處理輔料若只有三個組分����,第一個組分取全稱���,第二個組分取 2 個字���,第三個組分取 2-3 個字����;超過三個成分時�,第一個組分取全稱���,第二至第三組分取 2 個字���,第四組分后各取 1 個字���,如無特殊規定�,一般取中文首字�����。選詞組合的名稱應符合常用語言習慣��,避免不符合倫理學的組合名稱及其他不適宜的情況����。
③當共處理輔料的組分相同��,比例的次序相同但比例不同時���,不同的比例可不在名稱中體現�����,但應在產品的規格和標簽標識中加以注明��。
數據顯示���,2020年全球藥用輔料市場規模為873億美元��,預計2027年將達到1289億美元����,年復合增長率(CAGR)為5.57%(2021-2027)��。中國市場規模增長快速���,預計將由2020年的128億美元增長到2027年的210億美元��,年復合增長率為8.00%(2021-2027)(圖3)���。然而���,2017年我國藥用輔料市場規模在整個藥品制劑產值中僅為3-5%��,國外藥用輔料卻占整個藥品制劑產值的10-20%�,表明我國藥用輔料市場與國外相比還有較大差距��,但目前發展較快�����,未來前景廣闊���。

圖3. 2020~2027年中國藥用輔料市場規模及預測
在固體制劑開發中�,共處理輔料的應用給配方及工藝帶來了極大的便利�����。如在直壓工藝中����,共處理材料的流動性與可壓性��,大大簡化了輔料選擇�,提高了工藝穩定性�,從而節省了制造時間和成本����。
連續化生產是固體制劑開發未來的一個趨勢�。鑒于單一輔料性能的局限����,連續化生產工藝現在仍然極具挑戰性��。但共處理輔料的開發與應用�,對于連續化生產中所遇到的流動性����、可壓性以及均一性問題都帶來了極大的改善���,使連續化生產工藝變得更簡單��。
IID中大多數輔料的性質都是從GSRS中提取的�。盡管申請人可在原申請中提供輔料的商品名稱或通用名稱��,但IID會顯示輔料在GSRS中出現的首選術語��,以促進IID中命名的一致性����。GSRS首選術語通常用于識別單一成分物質���。當美國藥典/國家處方集(USP/NF)將輔料確定為單一成分物質時�,GSRS首選術語與該輔料的USP/NF專著標題相同���。然而����,如果USP/NF專著的標題涵蓋多種物質����,則GSRS對每種成分物質的首選術語可能與該專著有所不同��。在這種情況下���,IID中的首選術語和USP/NF專論標題可能有所不同����。
被USP/NF所收載的共處理輔料和輔料混合物通常在GSRS和IID中保留其專著名稱�,如果修改了專著標題����,則在GSRS和IID中進行更新��,以與USP/NF專著保持一致��。一個例子是乳化蠟���,這是一個具有USP/NF專著的輔料混合物�。該輔料以USP/NF名稱出現在IID中����。如果共處理的輔料或輔料混合物沒有USP/NF專著或GSRS首選術語�����,通常將根據其申請中提供的名稱或申請人提供的其他一些唯一標識碼在IID中列出�����。一個例子是輔料油酸甘油酯/丙二醇混合物���,它以申請人提供的名稱出現在IID中���。
未來:
隨著藥品制劑的研發創新以及質量要求的發展需要���,將對藥用輔料的有效性�����、經濟性����、安全性提出更高的要求���,發展以預混與共處理藥用輔料為代表的新型輔料勢在必行�����。而隨著生物科技���、納米技術�、3D 打印等新技術的應用��,此類藥用輔料的范圍和應用會進一步得到擴展��,其開發研究具有廣闊的市場前景����。共處理輔料在彌補藥物低機械性能�、難溶性���、均一性����、易成型性等方面展現了顯著的技術優勢�,為粉末直接壓片�、3D 打印技術等在更多藥物制劑的推廣應用提供了重要支撐�����;而這些新藥物制劑工藝的發展又能促進新型共處理輔料的研發與應用����。
目前隨著仿制藥一致性評價的常態化����,為應對仿制藥激烈競爭的挑戰�,生產制造商在輔料使用環節上降低成本正逐漸成為應對手段之一��。而使用可直接壓縮的結合劑進行藥物生產��,不僅可以降低成本���,而且在功能上有所增強��。使用多功能輔料也是另外一種解決辦法��,如一些輔料也可以被用作結合劑�、崩解劑和稀釋劑����,由于其具有強大的結合能力�����,不僅可提高藥片的生產量���,又可降低成本���。而隨著技術更新以及業界應用�����,部分預混與共處理輔料開始被中國藥典��、美國藥典和歐洲藥典越來越多的收載��,相關指導原則也相繼出臺���。但如何根據不同藥物制劑的生產要求��,重視和完善預混與共處理輔料的質量標準控制����,結合藥用輔料本身特性以及藥物與輔料相容性等特點[41]��,開展安全性和功能性風險評估與控制��,合理制定質量標準�,開展相關檢測方法研究��,從而保證藥物制劑的質量與療效的一致性���,則顯得尤為重要�����。世界各國正作出巨大努力�����,使藥用輔料的標準統一和完善���,從而為輔料的快速開發����、應用和審批鋪平道路���。

【收藏】優質藥用輔料關聯審評推薦——供外用/口服固體制劑應用篇①
